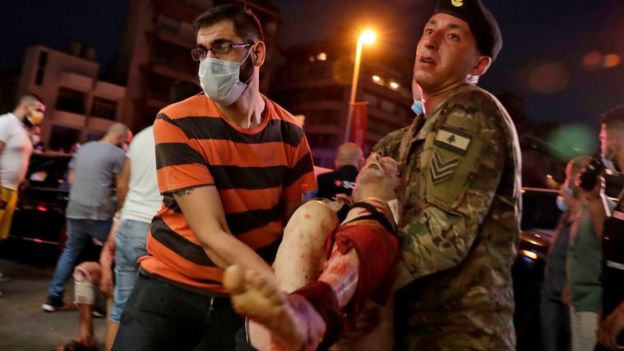
Las imágenes de la explosión de este martes en Beirut dieron la vuelta al mundo, y no es para menos.
La fuerza del estallido y la violencia de la nube expansiva en forma de hongo que se generó dan cuenta de lo peligroso que es el químico que reaccionó.
La explosión dejó más de un centenar de muertos, más de 5.000 heridos y decenas de miles de personas sin hogar.
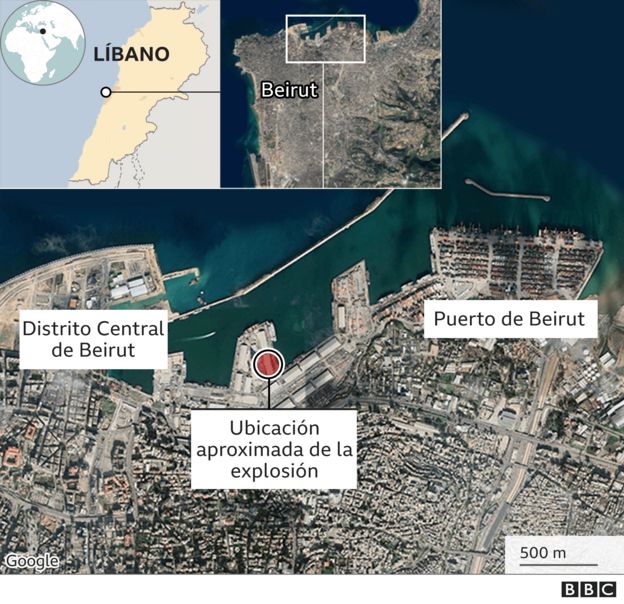
De hecho, la potencia de la explosión se sintió incluso a 240 kilómetros del puerto de Beirut, en la isla de Chipre.
La sustancia responsable fue nitrato de amonio, específicamente 2.750 toneladas que llevaban seis años almacenadas en el puerto de la capital del Líbano sin las medidas de seguridad adecuadas.
Así lo informaron el presidente del país, Michel Aoun, y su primer ministro, Hassan Diab.
Ahora resta por investigar qué hizo que el material prendiera y si se trató de un accidente, lo cual parece ser la teoría más probable hasta el momento.
¿Qué es y para qué se usa el nitrato de amonio?
El nitrato de amonio es un compuesto que ya ha demostrado su peligro en el pasado.
Se trata de un sólido cristalino que se fabrica en cantidades industriales y que se usa mayoritariamente como fuente de fertilizantes, pero también en la industria minera.
 Derechos de autor de la imagenGETTY IMAGES
Derechos de autor de la imagenGETTY IMAGES«El nitrato de amonio es uno de los fertilizantes más utilizados para la agricultura en todo el mundo. También se usa en la fabricación de explosivos», explicó a BBC Brasil Reinaldo Bazito, profesor del Instituto de Química de la Universidad de Sao Paulo.
Y añadió: «Es un explosivo altamente potente».
Según el experto, el nitrato de amonio suele almacenarse en grandes cantidades por la alta demanda de los agricultores para usarlo como fertilizante.
Sin embargo, Luiz Carlos Dias, profesor de Química de la Universidad de Campinas (Unicamp) de Brasil, aclaró que «para que haya una explosión, debe existir una combustión previa».
«Con una gran cantidad de producto almacenada, una temperatura superior a 300 grados puede hacerla explosiva. Un incendio puede alcanzar esa temperatura fácilmente», dijo Dias a BBC Brasil.
 Derechos de autor de la imagenGETTY IMAGES
Derechos de autor de la imagenGETTY IMAGESAl ser tan inflamable hay reglas muy estrictas para su almacenamiento seguro.
Entre los requisitos está que el lugar cuente con medidas a prueba de incendios. Tampoco puede haber desagües, tuberías u otros canales en los que se pueda acumular el nitrato porque crearía un peligro explosivo adicional.
Otro problema sucede cuando se deja el material sin usar por mucho tiempo porque «absorbe humedad y se convierte en una roca gigante», explicó a la BBC Andrew Sella, profesor de Química de la University College de Londres.
Esto es más peligroso, de acuerdo al académico, porque si se produce un choque, se expande mucho más fácil.
¿A qué se debió la rapidez con que se expandió la nube?
Tras la explosión, las imágenes desde Beirut mostraron una especie de nube con forma de hongo que se expandió rápidamente.

«Tienes una onda de choque supersónica que viaja a través del aire. La puedes ver en esa nube blanca esférica que viaja desde el centro y se expande hacia arriba», contó Sella.
La onda de choque se produce por el aire comprimido, explicó el profesor: «El aire se expande rápidamente, luego se enfría de repente y el agua se condensa, lo que origina la nube».
Según un artículo de la publicación académica digital The Conversation escrito por el ingeniero químico Gabriel da Silva, de la Universidad de Melbourne, Australia, una de las claves está en la densidad del oxígeno.
«El nitrato de oxígeno no se quema por sí solo», escribió Silva. «Actúa como una fuente de oxígeno que acelera la combustión de otros materiales».
«Las pastillas de nitrato de amonio tienen mucho más oxígeno concentrado que el aire que nos rodea. A altas temperaturas, este compuesto se descompone violentamente, creando gases como óxido de nitrógeno y vapor de agua», añadió.
Además del óxido de nitrógeno, cuando el nitrato de amonio explota, puede liberar otros gases tóxicos, como el amoníaco.
 Derechos de autor de la imagenGETTY IMAGES
Derechos de autor de la imagenGETTY IMAGESLos tintes naranjas que se vieron en la nube son causados por el dióxido de nitrógeno, el cual suele asociarse con la contaminación del aire.
«Si no hay mucho viento, podría convertirse en un peligro para las personas«, dijo Sella.
Silva coincidió: «Presentará un riesgo para la salud de los residentes hasta que se disipen naturalmente, lo que podría llevar varios días dependiendo del clima local».
Precedentes
Esta no es la primera vez que esta sustancia protagoniza episodios devastadores, tanto atentados como accidentes.
Argentina vivió el atentado más trágico de su historia un 18 de julio de 1994, cuando una explosión contra la Asociación Mutual Israelita Argentina (AMIA) dejó 85 muertos y más de 300 heridos.
A 26 años del caso, nadie ha sido juzgado o encarcelado.
 Derechos de autor de la imagenGETTY IMAGES
Derechos de autor de la imagenGETTY IMAGESSegún la justicia argentina, el atentado fue ejecutado por el grupo militante chiita Hezbolá, de origen libanés, bajo órdenes de Irán, algo que ese país siempre ha negado.
El nitrato de amonio fue justamente el explosivo utilizado en ese ataque.
También fue usado por Timothy McVeigh en un atentado que cometió en 1995 en la ciudad de Oklahoma, cuando creó una bomba con dos toneladas de nitrato de amonio, con la cual destruyó un edificio federal y mató a 168 personas.
Mucho antes, en 1921, 4.500 toneladas de nitrato de amonio causaron una explosión en una planta en Oppau, en Alemania, matando a más de 500 personas.
El accidente más mortífero ocurrió en Estados Unidos, en la Bahía Galveston, en Texas. Murieron al menos 581 personas tras la explosión de más de 2.000 toneladas del químico detonadas en un barco atracado en el puerto.
Recientemente, una explosión de nitrato de amonio y otros químicos mató a 173 personas en el puerto Tianjin, al norte de China.